1.

|
|
Balancee la ecuación siguiente: C6H14O + O2  CO2 + H2O CO2 + H2O
|
| 2C6H14O + 19O2  12CO2 + 14H2O 12CO2 + 14H2O |
| C6H14O + 9O2  6CO2 + 7H2O 6CO2 + 7H2O |
| C6H14O + (19/2)O2  6CO2 + 7H2O 6CO2 + 7H2O |
| 2C6H14O + 18O2  12CO2 + 14H2O 12CO2 + 14H2O |
| 2C6H14O + 4O2  2CO2 + 2H2O 2CO2 + 2H2O |
|
2.

|
|
Determine el peso formular aproximado del compuesto siguiente: Ca(C2H3O2)2
|
| 99 |
| 69 |
| 152 |
| 94 |
| 158 |
|
3.

|
|
Determine la fórmula empírica de un compuesto que contiene 52.9% de aluminio y 47.1% de oxígeno.
|
| AlO |
| Al2O3 |
| Al3O2 |
| Al0.53O0.47 |
| Al4O6 |
|
4.

|
|
El alcohol del “gasohol” se quema de acuerdo con la ecuación siguiente: C2H5OH + 3O2  2CO2 + 3H2O 2CO2 + 3H2O cuántos moles de CO2 se producen cuando se queman 3.00 mol de C2H5OH de esta manera.
|
| 3.00 mol |
| 6.00 mol |
| 2.00 mol |
| 4.00 mol |
| 1.50 mol |
|
5.

|
|
Un fabricante de bicicletas dispone de 5350 ruedas, 3023 marcos y 2655 manubrios. żCuántas bicicletas puede fabricar con estas partes?
|
| 2675 bicicletas |
| 2655 bicicletas |
| 3023 bicicletas |
| 5350 bicicletas |
|
6.

|
|
Balancee la ecuación siguiente: Al + Cr2O3  Al2O3 + Cr Al2O3 + Cr
|
| 2Al + Cr2O3  Al2O3 + 2Cr Al2O3 + 2Cr |
| 2Al + Cr2O3  Al2O3 + Cr Al2O3 + Cr |
| 4Al + 2Cr2O3  2Al2O3 + 4Cr 2Al2O3 + 4Cr |
| Al + Cr2O3  Al2O3 + 2Cr Al2O3 + 2Cr |
|
7.

|
|
Convierta la descripción siguiente en una ecuación balanceada: Cuando se hace pasar amoniaco gaseoso, NH3(g), sobre sodio caliente, se desprende hidrógeno gaseoso y se forma amida de sodio, NaNH2, como producto sólido. No olvide indicar el estado de cada compuesto.
|
| 2NH3 + Na  2NaNH2 + H2 2NaNH2 + H2 |
| NH3 + Na  NaNH2 + H2 NaNH2 + H2 |
| 2NH3 + 2Na  2NaNH2 + H2 2NaNH2 + H2 |
| 2NH3(g) + 2Na(s)  2NaNH2(s) + H2(l) 2NaNH2(s) + H2(l) |
| 2NH3(g) + 2Na(s)  2NaNH2(s) + H2(g) 2NaNH2(s) + H2(g) |
|
8.

|
|
Balancee la ecuación siguiente e indique si se trata de una reacción de combustión, de combinación o de descomposición: Li + N2  Li3N Li3N
|
| 6Li + N2  2Li3N, reacción de combinación 2Li3N, reacción de combinación |
| 6Li + N2  2Li3N, reacción de descomposición 2Li3N, reacción de descomposición |
| Li + N2  3Li3N, combinación 3Li3N, combinación |
| Li + N2  3Li3N, descomposición 3Li3N, descomposición |
| 6Li + N2  2Li3N, combusión 2Li3N, combusión |
|
9.

|
|
Balancee la ecuación siguiente e indique si se trata de una reacción de combustión, de combinación o de descomposición: H2O2(l)  H2O(l) + O2(g) H2O(l) + O2(g)
|
| H2O2(l)  H2O(l) + O2(g), reacción de descomposición H2O(l) + O2(g), reacción de descomposición |
| H2O2(l)  H2O(l) + (1/2)O2(g), reacción de combinación H2O(l) + (1/2)O2(g), reacción de combinación |
| H2O2(l)  H2O(l) + O2(g), reacción de combustión H2O(l) + O2(g), reacción de combustión |
| 2H2O2(l) 2H2O(l) + O2(g), reacción de descomposición 2H2O(l) + O2(g), reacción de descomposición |
| H2O2(l)  H2O(l) + (1/2)O2(g), reacción de descomposición H2O(l) + (1/2)O2(g), reacción de descomposición |
|
10.

|
|
El elemento oxígeno se compone de tres isótopos cuyas masas son de 15.994915, 16.999133 y 17.99916. Las abundancias relativas de estos tres isótopos son de 99.7587, 0.0374 y 0.2049, respectivamente. A partir de estos datos calcule la masa atómica media del oxígeno.
|
| 15.9563 |
| 15.9994 |
| 15.994915 |
| 16.00 |
| 15.9930 |
| 15.999377 |
|
11.

|
|
Con base en la fórmula estructural siguiente, calcule el porcentaje de carbono presente. (CH2CO)2C6H3(COOH)
|
| 64.70 por ciento |
| 66.67 por ciento |
| 69.25 por ciento |
| 76.73 por ciento |
|
12.

|
|
Una muestra de glucosa C6H12O6, contiene 4.0 x 1022 átomos de carbono. żCuántos átomos de hidrógeno y cuántas moléculas de glucosa contiene la muestra?
|
| 8.0 x 1022 atoms of H, 8.0 x 1022 moléculas de glucosa |
| 8.0 x 1022 átomos de H, 4.0 x 1022 moléculas de glucosa |
| 4.0 x 1022 átomos de H, 4.0 x 1022 moléculas de glucosa |
| 8.0 x 1022 átomos de H, 6.7 x 1021 moléculas de glucosa |
| 8.0 x 1022 átomos de H, 2.4 x 1023 moléculas de glucosa |
|
13.

|
|
żCuál es la masa en gramos de 0.257 mol de sacarosa,C12H22O11?
|
| 342 g |
| 7.51 x 10-5 g |
| 88.0 g |
| 8.80 g |
| 12.5 g |
|
14.

|
|
Calcule el número de moléculas presentes en una cucharada sopera de azúcar de mesa, C12H22O11,
|
| 6.02 x 1023 |
| 6.29 x 1024 |
| 1.85 x 1022 |
| 1.13 x 1023 |
| 3.01 x 1023 |
|
15.

|
|
Indique la fórmula empírica del compuesto siguiente si una muestra contiene 40.0 por ciento de C, 6.7 por ciento de H y 3.3 por ciento de O en masa.
|
| C4HO5 |
| CH20 |
| C2H4O2 |
| C3H6O3 |
|
16.

|
|
Cuál es la fórmula molecular del compuesto siguiente? fórmula empírica CH, masa molar 78 g/mol
|
| CH |
| C2H2 |
| C3H3 |
| C4H4 |
| C6H6 |
| C5H18 |
|
17.

|
|
El alcohol del “gasohol” se quema de acuerdo con la ecuación siguiente: C2H5OH + 3O2  2CO2 + 3H2O 2CO2 + 3H2O cuántos moles de CO2 se producen cuando se queman 3.00 mol de C2H5OH de esta manera?
|
| 6.00 g |
| 44.0 g |
| 0.130 g |
| 5.74 g |
| 2.87 g |
|
18.

|
|
La fermentación de glucosa, C6H12O6, produce alcohol etílico, C2H5OH, y dióxido de carbono: C6H12O6 (ac)  2C2H5OH(ac) + 2CO2(g) 2C2H5OH(ac) + 2CO2(g) żCuántos gramos de etanol se pueden producir a partir de 10.0 g de glucosa?
|
| 10.0 g |
| 2.56 g |
| 5.11 g |
| 4.89 g |
| 5.00 g |
|
19.

|
|
Las bolsas de aire para automóvil se inflan cuando se descompone rápidamente azida de sodio, NaN3, en los elementos que la componen según la reacción 2NaN3  2Na + 3N2 2Na + 3N2 żCuántos gramos de azida de sodio se necesitan para formar 5.00 g de nitrógeno gaseoso?
|
| 9.11 g |
| 8.81 g |
| 7.74 g |
| 3.33 g |
|
20.

|
|
El carburo de silicio, SiC, se conoce por el nombre común de carborundum. Esta dura sustancia, que se utiliza comercialmente como abrasivo, se prepara calentando SiO2 y C a temperaturas elevadas: SiO2(s) + 3C(s)  SiC(s) + 2CO(g) SiC(s) + 2CO(g) żCuántos gramos de SiC se pueden formar cuando se permite que reaccionen 3.00 g de SiO2 y 4.50 g de C?
|
| 2.00 g |
| 3.00 g |
| 5.01 g |
| 15.0 g |
|
21.

|
|
Balancee la ecuación siguiente: Mg3N2 + H2O  Mg(OH)2 + NH3 Mg(OH)2 + NH3
|
| Mg3N2 + 6H2O  3Mg(OH)2 + 2NH3 3Mg(OH)2 + 2NH3 |
| Mg3N2 + 2H2O  Mg(OH)2 + NH3 Mg(OH)2 + NH3 |
| Mg3N2 + 6H2O  3Mg(OH)2 + NH3 3Mg(OH)2 + NH3 |
| Mg3N2 + 3H2O  3Mg(OH)2 + 2NH3 3Mg(OH)2 + 2NH3 |
|
22.

|
|
Convierta lo siguiente en una ecuación química balanceada: Hidrógeno gaseoso reacciona con monóxido de carbono para formar metanol, CH3OH.
|
| H2 + CO  CH3OH CH3OH |
| 2H2 + CO2  CH3OH CH3OH |
| 4H + CO  CH3OH CH3OH |
| 2H2 + CO  CH3OH CH3OH |
|
23.

|
|
Balancee la ecuación siguiente e indique si se trata de una reacción de combustión, de combinación o de descomposición. H2O2 + SO2 H2SO4 H2SO4
|
| H2O2 + SO2  H2SO4, reacción de combinación H2SO4, reacción de combinación |
| H2O2 + SO2  H2SO4, reacción de descomposición H2SO4, reacción de descomposición |
| 2H2O2 + SO2  H2SO4, reacción de combinación H2SO4, reacción de combinación |
| 2H2O2 + SO2  H2SO4, reacción de descomposición H2SO4, reacción de descomposición |
|
24.

|
|
Balancee la ecuación siguiente: B10H18 + O2  B2O3 + H2O B2O3 + H2O
|
| B10H18 + 7O2  5B2O3 + 9H2O 5B2O3 + 9H2O |
| B10H18 + 19O2  10B2O3 + 9H2O 10B2O3 + 9H2O |
| B10H18 + 12O2  5B2O3 + 9H2O 5B2O3 + 9H2O |
| B10H18 + 9O2  5B2O3 + 9H2O 5B2O3 + 9H2O |
|
25.

|
|
El elemento cinc se compone de cinco isótopos cuyas masas son de 63.929, 65.926, 66.927, 67.925 y 69.925 uma. Las abundancias relativas de estos cinco isótopos son de 48.89, 27.81, 4.110, 18.57 y 0.62 por ciento, respectivamente. Con base en estos datos calcule la masa atómica media del zinc.
|
| 63.93 uma |
| 66.93 uma |
| 65.389 uma |
| 66.927 uma |
| 65.39 uma |
|
26.

|
|
Calcule el porcentaje de carbono presente en la cadaverina, C5H14N2, un compuesto presente en la carne en descomposición.
|
| 67.4 por ciento de C |
| 58.8 por ciento de C |
| 51.7 por ciento de C |
| 68.2 por ciento de C |
|
27.

|
|
Una muestra de vitamina A, C20H30O, contiene 4.0 x 1022 átomos de carbono. żCuántos átomos de hidrógeno y cuántas moléculas de vitamina A contiene la muestra?
|
| 6.0 x 1022 átomos de H, 4.0 x 1022 moléculas de vitamina A |
| 4.0 x 1022 átomos de H, 4.0 x 1022 moléculas de vitamina A |
| 6.0 x 1022 átomos de H, 2.0 x 1021 moléculas de vitamina A |
| 6.0 x 1022 átomos de H, 8.0 x 1023 moléculas de vitamina A |
|
28.

|
|
Calcule la masa en gramos de 0.0112 mol de beta 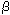 -fructosa, C6H12O6. -fructosa, C6H12O6.
|
| 0.0112 g |
| 180 g |
| 1.12 g |
| 2.02 g |
|
29.

|
|
Calcule el número de moléculas presentes en 6.2 g de formaldehído, CH2O.
|
| 6.0 x 1023 |
| 3.7 x 1024 |
| 1.2 x 1023 |
| 2.4 x 1023 |
|
30.

|
|
Indique la fórmula empírica del compuesto siguiente si una muestra contiene 57.9 por ciento de C, 3.6 por ciento de H y 38.6 por ciento de O en masa.
|
| C2HO |
| C4H3O2 |
| C8H6O4 |
| C12H9O6 |
|
31.

|
|
żCuál es la fórmula molecular del compuesto siguiente? fórmula empírica C2H3, masa molar 54 g/mol
|
| C2H3 |
| C4H6 |
| C6H9 |
| C8H12 |
|
32.

|
|
El octano se quema de acuerdo con la ecuación siguiente: 2C8H18 + 25O2  16CO2 + 18H2O 16CO2 + 18H2O żCuántos gramos de CO2 se producen cuando se queman 5.00 g de C8H18
|
| 40.0 g |
| 0.351 g |
| 15.4 g |
| 30.9 g |
|
33.

|
|
El CO2 que los astronautas exhalan se extraer de la atmósfera de la nave espacial por reacción con KOH: CO2 + 2KOH  K2CO3 + H2O K2CO3 + H2O żCuántos kg de CO2 se pueden extraer con 1.00 kg de KOH?
|
| 0.500 kg |
| 0.786 kg |
| 0.392 kg |
| 1.57 kg |
|
34.

|
|
Un producto secundario de la reacción que infla las bolsas de aire para automóvil es sodio, que es muy reactivo y puede encenderse en el aire. El sodio que se produce durante el proceso de inflado reacciona con otro compuesto que se agrega al contenido de la bolsa, KNO3, según la reacción 10Na + 2KNO3  K2O + 5Na2O + N2 K2O + 5Na2O + N2 żCuántos gramos de KNO3 se necesitan para eliminar 5.00 g de Na?
|
| 110 g |
| 2.20 g |
| 4.40 g |
| 1.00 g |
|
35.

|
|
En la reacción 3NO2 + H2O  2HNO3 + NO, żcuántos gramos de HNO3 se pueden formar cuando se permite que reaccionen 1.00 g de NO2 y 2.25 g de H2O? 2HNO3 + NO, żcuántos gramos de HNO3 se pueden formar cuando se permite que reaccionen 1.00 g de NO2 y 2.25 g de H2O?
|
| 0.913 g |
| 0.667 g |
| 15.7 g |
| 1.37 g |
|
36.

|
|
Escriba la ecuación balanceada de la reacción que se produce cuando se calienta nitrato de potasio sólido y éste se descompone para formar nitrito de potasio sólido y oxígeno gaseoso.
|
| 2 KNO4(s)  2 KNO3(s) + O2(g) 2 KNO3(s) + O2(g) |
| 2 KNO3(s)  2 KNO2(s) + O2( g) 2 KNO2(s) + O2( g) |
| 2 KNO3  2 KNO2 + O2 2 KNO2 + O2 |
| KNO3(s)  KNO2(s) + (1/2)O2(g) KNO2(s) + (1/2)O2(g) |
|
37.

|
|
żCuál es la fórmula empírica de un compuesto que contiene 7.989 g de carbono y 2.011 g de hidrógeno?
|
| C2H5 |
| C3H |
| C8H2 |
| CH3 |
| C2H6 |
|
38.

|
|
Si 3.00 mol de SO2 gaseoso reaccionan con oxígeno para producir trióxido de azufre, żcuántos moles de oxígeno se necesitan?
|
| 3.00 mol O2 |
| 6.00 mol O2 |
| 1.50 mol O2 |
| 4.00 mol O2 |
|
39.

|
|
żCuántos gramos de óxido de hierro Fe2O3, se pueden producir a partir de 2.50 g de oxígeno que reaccionan con hierro sólido?
|
| 12.5 g |
| 8.32 g |
| 2.50 g |
| 11.2 g |
|
40.

|
|
Cuando se prepara H2O a partir de hidrógeno y oxígeno, si se parte de 4.6 mol de hidrógeno y 3.1 mol de oxígeno, żcuántos moles de agua se pueden producir y qué permanece sin reaccionar?
|
| se producen 7.7 mol de agua y quedan 0.0 mol de O2 |
| se producen 3.1 mol de agua y quedan 1.5 mol de O2 |
| se producen 2.3 mol de agua y quedan 1.9 mol de O2 |
| se producen 4.6 mol de agua y quedan 0.8 mol de O2 |
| se producen 4.6 mol de agua y quedan 0.0 mol de O2 |

