1.

|
|
żAumenta, disminuye o no cambia el pH al agregar cada una de las sustancias siguientes? (i) NaNO2 a una solución de HNO2, (ii) HCl a una solución de NaC2H3O2
|
| (i) disminuye, (ii) aumenta |
| (i) aumenta, (ii) aumenta |
| (i) disminuye, (ii) disminuye |
| (i) aumenta, (ii) disminuye |
| (i) aumenta, (ii) no cambia |
|
2.

|
|
Calcule el pH de una solución de propionato de potasio, KC3H5O2, y ácido propiónico, HC3H5O2 (Ka = 1.3 x 10-5).
|
| 6.5 x 10-6 |
| 2.6 x 10-5 |
| -4.59 |
| 4.59 |
| 5.19 |
| 10.56 |
|
3.

|
|
Calcule el porcentaje de ionización del ácido butanoico 0.10 M (Ka = 1.5 x 10-5) en una solución 0.050 M de butanoato de sodio.
|
| 3.0 x 10-5 |
| 3.0 x 10-4 |
| 3.0 x 10-2 |
| 4.52 |
|
4.

|
|
Calcule el pH de una solución amortiguadora que es 0.20 M en ácido fórmico y 0.15 M en formiato de sodio (Ka = 1.8 x 10-4).
|
| 2.4 x 10-4 |
| 0.70 |
| 0.82 |
| 3.62 |
| 8.33 |
|
5.

|
|
żCuántos moles de hipobromito de sodio, NaBrO, se deben agregar a 1.00 L de ácido hipobromoso, HBrO, (Ka = 2.5 x 10-9), para formar una solución amortiguadora de pH 8.80? Suponga que el volumen no cambia con la adición de NaBrO.
|
| 0.13 mol |
| 0.20 mol |
| 0.32 mol |
| No se puede formar una solución amortiguadora con este pH. |
|
6.

|
|
żCuál es la proporción de [HCO3-] a [H2CO3] en la sangre a un pH de 7.40 (Ka = 4.3 x 10-7)?
|
| 1.7 x 10-14 |
| 7.0 x 10-4 |
| 9.3 x 10-2 |
| 11 |
|
7.

|
|
żCuántos mL de NaOH 0.0350 M se necesitan para titular 65.0 mL de HBr 0.0620 M hasta el punto de equivalencia?
|
| 8.69 x 10-3 mL |
| 33.4 mL |
| 36.7 mL |
| 115 mL |
|
8.

|
|
Una muestra de 50.0 mL de ácido acético, HC2H3O2, se titula con una solución de NaOH 0.150 M. Calcule el pH después que se han agregado 25.0 mL de base (Ka = 1.8 x 10-5).
|
| 0.55 |
| 2.52 |
| 2.62 |
| 3.92 |
| 3.99 |
|
9.

|
|
Si la solubilidad molar del CaF2 a 35°C es de 1.24 x 10-3 mol/L, żcuál es la Ksp a esta temperatura?
|
| 1.91 x 10-9 |
| 7.63 x 10-9 |
| 1.54 x 10-6 |
| 3.08 x 10-6 |
|
10.

|
|
Calcule la solubilidad molar del Cu(OH)2 a un pH de 9.0 (Ksp = 2.2 x 10-20).
|
| 2.2 x 10-30 |
| 2.2 x 10-15 |
| 2.2 x 10-10 |
| 2.2 x 10-11 |
| 2.2 x 10-2 |
|
11.

|
|
La Ksp del AgI = 8.3 x 10-17, y la Kf del Ag(CN)2- es = 1.0 x 1021. Calcule la constante de equilibrio de la reacción siguiente: AgI(s) + 2CN-(ac) 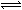 Ag(CN)2- (ac) + I- (ac) Ag(CN)2- (ac) + I- (ac)
|
| 8.3 x 20-38 |
| 8.3 x 10-17 |
| 1.2 x 10-5 |
| 8.3 x104 |
| 1.0 x 1021 |
|
12.

|
|
żPrecipitará Mn(OH)2 de la solución si se ajusta el pH de una solución de MnCl2 0.050 M a 8.0 (Ksp = 1.8 x 10-11)?
|
| no |
| sí |
|
13.

|
|
Calcule el pH mínimo necesario para precipitar el Ni(OH)2 de manera tan completa que la concentración de Ni2+ sea de menos de 1.0 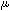 g/L (1000 partes por billón(ppb) (Ksp = 1.6 x 10-14). g/L (1000 partes por billón(ppb) (Ksp = 1.6 x 10-14).
|
| 2.90 |
| 7.10 |
| 8.20 |
| 9.60 |
| 11.00 |
|
14.

|
|
Cuando se trata con ácido diluido una solución que contiene un número desconocido de iones metálicos, no se forma un precipitado. Se ajusta el pH a alrededor de 1 y se burbujea H2S y tampoco se forma un precipitado. En seguida se ajusta el pH de la solución a 8 aproximadamente y de nuevo se burbujea H2S En este caso se forma un precipitado. Se trata el filtrado de esta solución con (NH4)2HPO4. No se forma un precipitado. żCuáles de los iones metálicos estudiados en la Sección 17.7 están presentes posiblemente?
|
| Grupo 3 y Grupo 5 |
| Grupo 3 |
| Grupo 2 y Grupo 5 |
| Grupo 4 |
|
15.

|
|
En el curso de varios procedimientos de análisis cualitativo se encuentra la mezcla siguiente: Mg2+ y K+. Sugiera un método para separar esta mezcla.
|
| agregar HCl diluido |
| agregar HCl 0.2 M y H2S |
| agregar (NH4)2S a pH 8 |
| agregar (NH4)2HPO4 a una solución básica |
| no es posible separar los iones |
|
16.

|
|
żQué pH se necesita para precipitar el Ni(OH)2 de forma tan completa que la concentración de níquel sea menor que 1.1 x 10-5 M (Ksp = 1.6 x 10-14)?
|
| 1.6 x 10-5 |
| 3.8 x 10-5 |
| 9.58 |
| 4.42 |
|
17.

|
|
żCuál o cuáles de los iones siguientes tienen hidróxidos y óxidos anfotéricos?
|
| Fe3+ |
| Al3+, Cr3+ |
| Ca2+ |
| Pb2+ |
| Na+, K+, Ag+ no son llamados iones |
|
18.

|
|
żCuál de los cambios siguientes es incorrecto?
|
| El HNO3 agregado a CaC2H3O2 reduce el pH |
| El CaCl2 agregado a una solución de HCl no cambia el pH |
| El KNO3 agregado a una solución de HCl no cambia el pH |
| El NaC2H3O2 agregado a una solución de HC2H3O2 eleva el pH |
| el NaBr agregado a una solución de HBr eleva el pH |
|
19.

|
|
żCuál de las acciones siguientes reduce el pH de una solución de ácido cítrico?
|
| adición de iones acetato |
| adición de ácido cítrico |
| adición de iones citrato |
| adición de iones cloruro |
| adición de iones nitrato |
|
20.

|
|
żCuál es el pH de una solución que contiene una concentración inicial de ácido cítrico 0.080 M y de iones citrato 0.010 M (Ka = 7.4 x 10-4)?
|
| 2.11 |
| 2.23 |
| 1.10 |
| 2.40 |
|
21.

|
|
żCuál es el pH de una solución que contiene una concentración inicial de ácido oxálico 0.25 M y de ion oxalato 0.35 M (Ka = 5.9 x 10-2).
|
| 0.92 |
| 1.38 |
| 1.48 |
| 0.60 |
|
22.

|
|
El ácido láctico es un ácido monoprótico con una Ka of 1.4 x 10-4. żCuál es el porcentaje de ionización de una solución de ácido láctico 0.100 M en ausencia y en presencia de lactato de sodio 0.0500 M?
|
| 0.37 por ciento, 0.028 por ciento |
| 1.2 por ciento, 0.28 por ciento |
| 3.7 por ciento, 0.28 por ciento |
| 3.7 por ciento, 3.7 por ciento |
|
23.

|
|
żCuál es el pH de una solución amortiguadora preparada a partir de ácido fórmico 0.30 M y formiato de potasio 0.15 M (Ka = 1.8 x 10-4)?
|
| 1.87 |
| 3.44 |
| 2.13 |
| 4.05 |
| 3.77 |
|
24.

|
|
Una solución amortiguadora contiene ácido acético 0.30 M y acetato de sodio 0.20 M. żCuál es el pH de la solución amortiguadora recién preparada y después de agregar 0.030 mol/L de un ácido fuerte o 0.030 mol/L de una base fuerte (Ka = 1.8 x 10-5)?
|
| 4.92, 5.03 con ácido, 4.81 con base |
| 4.56, 4.56 con ácido, 4.56 con base |
| 4.56, 4.46 con ácido, 4.68 con base |
| 4.74, 4.61 con ácido, 4.88 con base |
| 4.56, 4.68 con ácido, 4.46 con base |
|
25.

|
|
Se necesita preparar una solución amortiguadora con un pH de 3.50 a partir de ácido cítrico y dihidrógeno citrato de sodio. Si no se toman en cuenta las ionizaciones superiores del ion dihidrógeno citrato, żqué concentración de dihidrógeno citrato de sodio es necesario agregar al ácido 0.40 M (Ka = 7.4 x 10-4)?
|
| 0.40 M |
| 1.00 M |
| 0.20 M |
| 1.40 M |
| 0.94 M |
|
26.

|
|
żQué proporción de la concentración de ion bicarbonato a la concentración de ácido carbónico es necesaria para tener una solución amortiguadora con un pH de 7.00 (Ka = 4.3 x 10-7)?
|
| 1.0 |
| 4.3 |
| 2.0 |
| 3.0 |
| 0.23 hydroxido por Mg(OH)2. |
|
27.

|
|
żCuántos mL de HCl 0.250 M se necesitan para neutralizar 1.20 g de Mg (OH)2 en 200 mL de agua?
|
| 82.3 mL |
| 10.2 mL |
| 165 mL |
| 9.6 L |
| 200. mL |
|
28.

|
|
żCuántos mL de NaOH 0.150 M se necesitan para titular 21.50 mL de una solución de ácido acético 0.120 M?
|
| 17.2 mL |
| 26.9 mL |
| 34.4 mL |
| este cálculo no es posible porque el ácido acético es un ácido débil. |
|
29.

|
|
Si S es la solubilidad de una sal en moles por litro, żcuál de las expresiones de Ksp es incorrecta?
|
| AgS -- Ksp = S2 |
| AgCl -- Ksp = S2 |
| BaSO4 -- Ksp = S2 |
| Cu(OH)2 -- Ksp = 4S3 |
| Ca3(PO4)2 -- Ksp = 16S5 |
|
30.

|
|
La solubilidad del sulfato de plomo es de 4.25 mg por 100 mL de solución. żCuál es su Ksp?
|
| 1.40 x 10-4 |
| 1.81 x 10-3 |
| 1.96 x 10-8 |
| 7.86 x 10-8 |
| 1.96 x 10-10 |
|
31.

|
|
Si la solubilidad molar del CaF2 es de 1.24 x 10-3 mol/L, żcuál es su Ksp?
|
| 1.24 x 10-3 |
| 1.91 x 10-9 |
| 3.81 x 10-9 |
| 7.63 x 10-9 |
| 4.77 x 10-10 |
|
32.

|
|
Calcule la solubilidad en mol/L del Cu(OH)2 a pH = 7.0. Ksp = 2.2 x 10-20.
|
| 1.77 x 10-7 |
| 2.2 x 10-6 |
| 5.5 x 10-7 |
| 4.4 x 10-6 |
| 2.1 x 10-4 |
|
33.

|
|
żEn qué caso o casos se forma un precipitado? (i) una solución de 0.050 M MnCl2 con pH = 8.00 (Precipita Mn(OH)2) Ksp = 1.9 x 10-13. (ii) se agregan 100. mL de 0.010 M AgNO3 a 20. mL de .050 M Na2SO4 (Precipita Ag2SO4) Ksp = 1.4 x 10-5.
|
| i -- no, ii -- no |
| i -- no, ii -- sí |
| i -- sí, ii -- no |
| i -- sí, ii -- sí |
|
34.

|
|
żEn cuál o cuáles de las soluciones siguientes se forma un precipitado? (i) una solución de AgNO3 agregada a una solución de NaCl (ii) iones S2- agregados a una solución de Cu2+ (iii) iones fosfato agregados a una solución que contiene Mg2+ (iv) Cu2+ agregado a una solución que contiene Mg2+
|
| i, ii, y iii |
| todas forman precipitados |
| i y iii |
| ii y iii |
| iii y iv |
| ii y iv |

